
海思科晚间公告,公司于近日收到美国食品药品监督管理局(简称“FDA”)的Study May Proceed Letter,根据FDA相关规定,经审查,公司2025年5月递交的HSK47388片临床试验申请符合药品注册的有关要求,同意本品开展临床试验。HSK47388片拟用于自身免疫疾病的治疗。
举报 第一财经广告合作,请点击这里此内容为第一财经原创,著作权归第一财经所有。未经第一财经书面授权,不得以任何方式加以使用,包括转载、摘编、复制或建立镜像。第一财经保留追究侵权者法律责任的权利。如需获得授权请联系第一财经版权部:banquan@yicai.com 相关阅读 去年我国新药临床试验数量再创新高,司美格鲁肽领跑
去年我国新药临床试验数量再创新高,司美格鲁肽领跑2024年,我国新药注册临床试验数量为近五年新高,将近5000项(4900项),较上一年增长了13.9%。
9 649 06-20 10:52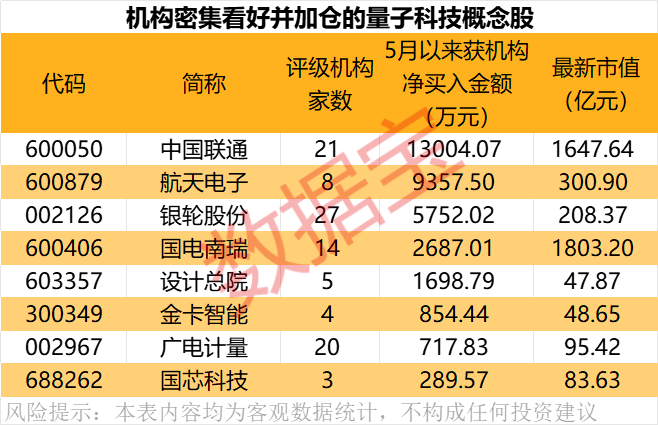 量子科技产业潜力巨大 机构密集看好并加仓的量子科技概念股出炉
量子科技产业潜力巨大 机构密集看好并加仓的量子科技概念股出炉量子科技产业潜力巨大 机构密集看好并加仓的量子科技概念股出炉
17 06-17 08:04 创新药临床试验审评审批提速,一类创新药等纳入30日通道
创新药临床试验审评审批提速,一类创新药等纳入30日通道此次征求意见稿,拟统一符合资质要求的药物范畴,并在“生物制品1类创新药”的基础上,还明确纳入符合要求的“中药”“化学药品”。
481 06-16 18:11 晚间公告丨6月15日这些公告有看头
晚间公告丨6月15日这些公告有看头6月15日晚间,沪深两市多家上市公司发布公告,以下是第一财经对一些重要公告的汇总,供投资者参考。
932 06-15 19:11 连续3年ROE超10% 未来高成长的超跌优质科技股
连续3年ROE超10% 未来高成长的超跌优质科技股连续3年ROE超10% 未来高成长的超跌优质科技股
0 06-12 12:48 一财最热 点击关闭启泰网配资-股票查询网-云南炒股配资-个人配资提示:文章来自网络,不代表本站观点。